Imiter la nature pour améliorer la santé

- Un poison qui traverse les barrières
- Une peau artificielle inspirée des moules
- Leçons de mobilité du poisson zèbre
Régénérer la peau ou transporter des médicaments vers des zones spécifiques de notre organisme est aujourd'hui possible grâce à l'inspiration que les scientifiques trouvent dans la nature. Trois projets soutenus par les appels à projets CaixaResearch pour la recherche et l'innovation en santé étudient si des animaux tels que les moules, les poissons zèbres ou les abeilles détiennent certaines des clés pour traiter des maladies qui constituent un défi pour la communauté médicale internationale.
Au cours de milliards d'années d'évolution, la nature a généré des solutions qui permettent aux êtres vivants de s'adapter à leur environnement et de survivre. Les êtres humains peuvent-ils apprendre de ceux qui ont déjà une expérience avérée dans la création de solutions innovantes et efficaces ? C'est précisément ce que fait le biomimétisme, une discipline qui se concentre sur l'amélioration de la vie humaine par l'étude et la recréation de structures biologiques et de leurs fonctions.
En effet, bon nombre des réponses aux problèmes auxquels nous sommes confrontés aujourd'hui pourraient se trouver dans la nature, comme l'ont déjà fait Léonard de Vinci, qui s'est inspiré des oiseaux pour concevoir des machines volantes, ou Alexander Fleming, dont la découverte de la pénicilline est née en observant comment un champignon inhibait la croissance des bactéries, ce qui a donné naissance aux antibiotiques et révolutionné la médecine.
Dans le domaine biomédical, le biomimétisme a eu un impact considérable ces dernières années, avec des avancées importantes pour la santé humaine. Les scientifiques ont réussi à développer des matériaux biocompatibles, à réaliser des progrès considérables en médecine régénérative et même à acheminer certains médicaments vers des zones spécifiques de l'organisme pour y appliquer un traitement.
Un poison qui traverse les barrières
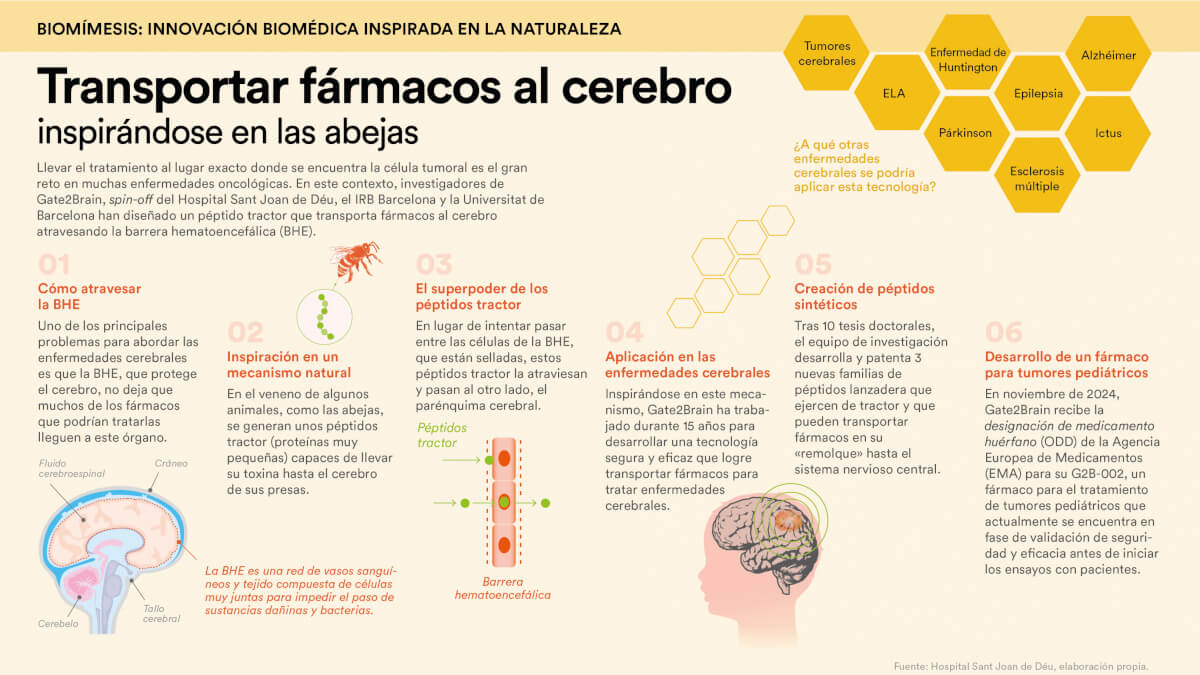
Amener le traitement à l'endroit exact où se trouve la cellule tumorale est le grand défi dans de nombreuses maladies oncologiques. À cet égard, des chercheurs de Gate2Brain, une spin-off de l'hôpital Sant Joan de Déu, de l'IRB Barcelona et de l'Université de Barcelone, ont conçu un peptide tracteur qui transporte des médicaments vers le cerveau et traverse la barrière hémato-encéphalique (BHE). Cette technologie permettra d'améliorer le traitement des maladies du cerveau, notamment le cancer du cerveau chez les enfants, en optimisant l'acheminement des médicaments vers cet organe.
Si plusieurs médicaments avaient jusqu'à présent démontré une puissante activité antitumorale, tous avaient échoué lors des essais cliniques car ils ne pouvaient pas traverser la BHE pour atteindre la tumeur. « Il s'agit d'une barrière cellulaire protectrice qui ne laisse entrer dans le système nerveux central que certaines molécules du sang circulant afin d'empêcher l'entrée d'agents pathogènes et d'autres substances nocives », explique la Dre Meritxell Teixidó, PDG et cofondatrice de Gate2Brain, qui bénéficie de la collaboration de l'Unité de recherche sur le cancer infantile - Fondation « la Caixa » de l'hôpital Sant Joan de Déu.
L'équipe dirigée par Teixidó, qui a bénéficié du soutien de RecerCaixa, CaixaImpulse Validate et CaixaImpulse Consolidate, a étudié le potentiel des peptides présents dans le venin des scorpions et des abeilles pour fonctionner comme des tracteurs moléculaires. « Nous recherchions des peptides, qui sont de très petites protéines, capables d'agir comme des tracteurs moléculaires pour transporter le médicament jusqu'au cerveau ; et nous avons constaté que l'abeille, comme beaucoup d'autres animaux, génère dans son venin un peptide tracteur qui transporte sa toxine jusqu'au système nerveux central, mais qui pourrait également transporter des médicaments pour soigner », explique-t-elle. « Ces tracteurs ne passent pas entre les cellules de la BHE, qui sont scellées, mais pénètrent à l'intérieur et ressortent de l'autre côté, dans le parenchyme cérébral », précise-t-elle.
En général, améliorer l'arrivée du médicament au cerveau présente des avantages significatifs pour le patient, car l'administration de la dose exacte améliore l'efficacité du traitement et réduit les effets secondaires.
En outre, les résultats obtenus pourraient être appliqués à d'autres agents thérapeutiques et barrières biologiques, avec des implications cliniques importantes. « Il existe de nombreux candidats médicaments pour les maladies du cerveau, mais 98 % d'entre eux auront besoin d'un tracteur. Notre technologie pourrait être appliquée à bon nombre d'entre eux », certifie la chercheuse.
En novembre 2024, Gate2Brain a franchi une étape décisive dans la lutte contre les tumeurs cérébrales pédiatriques en obtenant la désignation de médicament orphelin (Orphan Drug Designation, ODD) de l'Agence européenne des médicaments (EMA) pour son produit innovant, G2B-002. Le projet est actuellement en phase préclinique réglementaire, à un stade de transition entre les essais sur les rongeurs et les non-rongeurs (les porcs, plus précisément). « Même si l'essai clinique est prévu dans trois ans, nous sommes à un moment très important pour cette technologie et ce premier produit », ajoute le Dr Teixidó.
Son équipe travaille sans relâche pour ouvrir une nouvelle ère d'options thérapeutiques dans un domaine où les besoins sont importants et non satisfaits. « Ces dernières années, des progrès considérables ont été réalisés dans le diagnostic des tumeurs cérébrales, dans les thérapies plus avancées, mais surtout dans la connaissance de ces tumeurs afin de pouvoir proposer une médecine beaucoup plus personnalisée ; et les tracteurs pourraient être l'ingrédient qui aidera ces thérapies à mieux atteindre leur but », conclut-elle.

Une peau artificielle inspirée des moules
La création d'une peau artificielle est un besoin médical de premier ordre. Le processus de cicatrisation des plaies cutanées, telles que les brûlures ou les ulcères (très fréquentes dans des maladies comme le diabète), est lent et complexe, et malheureusement, il est souvent ralenti, voire bloqué, par l'absence de traitements efficaces.
L'équipe de Salvio Suárez, chercheur à l'Institut catalan des nanosciences et des nanotechnologies (ICN2), a mis au point une famille de membranes artificielles, bioinspirées de la capacité des moules à adhérer sous l'eau, qui ont déjà été validées dans des études précliniques pour la régénération du cartilage et de la peau. Les nouveaux matériaux adhèrent aux tissus biologiques, sont bioabsorbables, possèdent des propriétés antimicrobiennes et sont capables de transférer des cellules vers les tissus endommagés, favorisant ainsi leur régénération.
Comme l'explique Suárez, « nous nous sommes d'abord concentrés sur le cartilage et avons constaté que la régénération était très positive, ce qui nous a amenés à la régénération de la peau, car cela nous permettait d'étudier la membrane à plus grande échelle ». Ils ont ensuite mené une deuxième étude préclinique sur la régénération des plaies courantes et ont constaté qu'ils pouvaient réduire de moitié le temps nécessaire à leur guérison. Ils sont actuellement engagés dans un deuxième essai préclinique sur des porcs, « car les caractéristiques de la peau de ces animaux sont plus proches de celles de la peau humaine ».
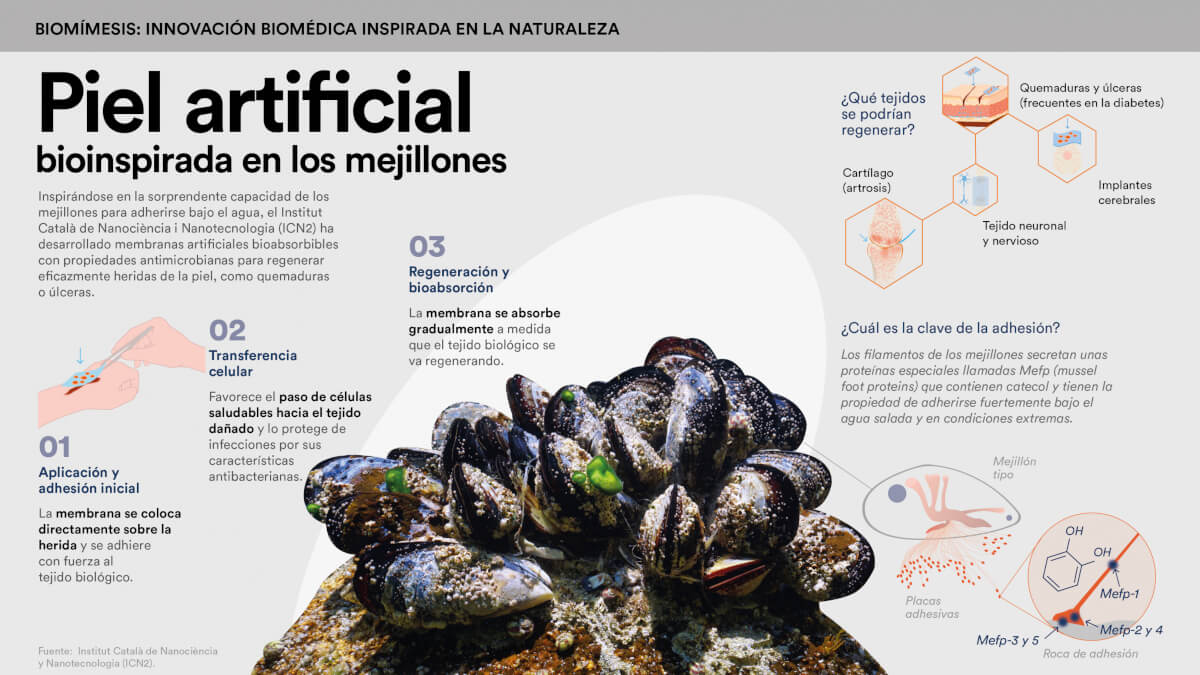
Ce projet, soutenu par l'appel à projets CaixaImpulse pour l'innovation dans le domaine de la santé, vise à optimiser et à valider des membranes artificielles qui ont à la fois des capacités régénératrices et antibactériennes. « Les propriétés antimicrobiennes sont dues aux molécules des moules qui nous ont inspirés », explique l'expert en science des matériaux. Leur avantage est qu'elles ont la capacité de s'oxyder avec le temps. « Les membranes que nous produisons, inspirées de ces molécules, s'oxydent également et génèrent des espèces chimiques, telles que le peroxyde d'hydrogène [l'eau oxygénée], qui ont des propriétés désinfectantes ». De plus, ce mécanisme antimicrobien n'a pas encore généré de résistance chez les bactéries. « Par conséquent, nous disposons d'un large spectre d'action, même pour les bactéries multirésistantes », assure Suárez.
Cette technique révolutionnaire peut réduire la durée d'hospitalisation, diminuer les infections, très fréquentes chez les patients brûlés, et, à terme, minimiser également le rejet de la greffe. « Ce que nous recherchons », souligne le chercheur, « c'est que cette nouvelle peau ressemble autant que possible à l'originale. D'un point de vue fonctionnel, nous avons réussi à lui conférer des propriétés similaires en termes de souplesse, de perméabilité et de sensibilité ».
Les chercheurs envisagent également d'étendre son utilisation potentielle au traitement d'autres maladies. « Nous validons actuellement ses propriétés pour la régénération neuronale et également pour le traitement de certains types de tumeurs », assure-t-il.
L'objectif final est de mener un premier essai clinique chez l'homme. « Nous espérons pouvoir commencer le recrutement des patients au cours du second semestre 2026 », conclut-il. De plus, les chercheurs viennent de créer la société Tirecat Health SL afin de poursuivre ce développement et celui d'autres applications de leur technologie.

Leçons de mobilité du poisson zèbre
Selon l'Organisation mondiale de la santé (OMS), jusqu'à un demi-million de personnes dans le monde souffrent chaque année d'une lésion de la moelle épinière. Les programmes de rééducation peuvent aider à récupérer certaines fonctions et à réduire le risque de complications, mais à ce jour, il n'existe aucun traitement capable de réparer les lésions permanentes.
Récemment, un projet soutenu par l'appel à projets CaixaResearch pour la recherche en santé, en collaboration avec la Fundação para a Ciência e a Tecnologia (FCT), a identifié de nouveaux traitements potentiels.
Leonor Saúde, chercheuse au Gulbenkian Institute for Molecular Medicine de Lisbonne, est spécialisée en biologie du développement et a largement étudié les processus embryonnaires du poisson zèbre. Elle et son équipe ont remarqué une capacité surprenante chez ce petit poisson d'eau douce : deux à trois semaines après avoir subi une lésion médullaire, il recommence à nager normalement, car il retrouve la mobilité et la sensibilité dans la zone touchée. En revanche, les mammifères tels que les souris ne présentent généralement que très peu d'amélioration pendant cette période. « Nous y avons vu une opportunité d'acquérir de nouvelles connaissances qui pourraient un jour être appliquées à des patients atteints de lésions de la moelle épinière », explique-t-elle.

L'équipe de Saúde a étudié minutieusement les deux animaux afin de déterminer la cause de ces résultats si disparates. Ils ont observé que les poissons zèbres, qui ne cessent jamais de grandir, ne cessent jamais de créer des neurones, de sorte que s'ils subissent une lésion de la moelle épinière, ils peuvent remplacer les neurones perdus par de nouveaux. « Ils ne forment pas non plus de cicatrice autour de la lésion et ne souffrent pas d'inflammation chronique », explique l'experte.
Cependant, la grande surprise pour l'équipe a été « la quantité inégale de cellules sénescentes dans chacun des modèles », révèle Saúde. « Il s'agit de cellules qui s'accumulent avec l'âge dans tous les tissus de l'organisme. Ainsi, d'une certaine manière, la sénescence est un indicateur du vieillissement. Chez les poissons zèbres, ces cellules disparaissent des tissus 30 jours après la lésion. Chez les modèles murins, en revanche, elles s'accumulent dans la zone lésée ».
L'équipe de cette chercheuse a décidé d'utiliser un médicament sénolytique pour réduire le nombre de cellules vieillissantes chez des souris présentant des lésions de la moelle épinière et a découvert que la récupération motrice et sensorielle s'améliorait. « Nous avons conclu que ces cellules ont un effet négatif sur les lésions médullaires : elles aggravent considérablement la récupération car elles sécrètent des molécules inflammatoires et profibrotiques, qui contribuent à l'inflammation et à la formation de cicatrices », précise-t-elle.

« Nous menons actuellement des expériences de séquençage d'ARN de cellules individuelles afin de mieux caractériser ces cellules et leur phénotype sécrétoire [l'ensemble des molécules qu'elles sécrètent] à des moments précis après une lésion », ajoute l'experte. Son objectif est de comprendre quel type de cellules elles étaient avant de devenir sénescentes, d'identifier les molécules qu'elles produisent et de concevoir des stratégies plus précises pour manipuler ces facteurs et réduire leur impact négatif sur les tissus.
À l'avenir, la chercheuse prévoit que, s'agissant d'une affection médicale très complexe, le traitement de ce type de lésions combinera des thérapies telles que la neuroprotection, la neurostimulation, la greffe de cellules souches et peut-être d'autres que nous ne connaissons pas encore.
La collaboration s'est toujours révélée être un moteur essentiel du progrès scientifique, mais ce n'est pas le seul. Comme le montrent ces trois recherches, la nature joue également un rôle fondamental. Et elle continuera à le faire. En effet, « il y a à peine trois ans, on a découvert qu'il existait un mammifère, l'Acomys ou souris épineuse, qui, contrairement aux autres, était capable de régénérer sa moelle épinière », révèle Saúde. « Les recherches se poursuivent pour comprendre pourquoi, mais il est clair que les scientifiques doivent continuer à se tourner vers la nature pour apprendre d'elle », conclut-elle.